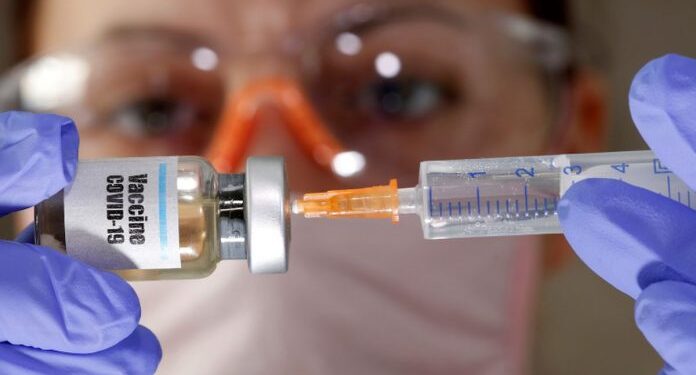
El tratamiento desarrollado por la Universidad de Oxford acumula errores y polémicas, con un uso muy dispar: suspendido en Sudáfrica y con restricciones de edad en Europa. ¿Qué ha ocurrido?
Hace unos meses no sabíamos si íbamos a tener vacuna contra el covid, ni cuándo ni cómo. Sin embargo, el proyecto de la Universidad de Oxford, aliada con la farmacéutica AstraZeneca, también británica, comenzó a destacar desde el principio. La investigación no solo iba bien, con su propuesta basada en el uso de un adenovirus de chimpancé, sino que parecía la apuesta más ambiciosa y altruista: querían llegar a todo el mundo al menor precio posible porque no buscaban beneficios. Con una rapidez extraordinaria, desarrollaron el candidato a vacuna y realizaron los primeros ensayos clínicos. En pleno verano ya habían comenzado la fase 3 con miles de voluntarios de varios países. Sin embargo, a partir de ahí todo comenzó a torcerse.
Los ensayos se suspendieron temporalmente por una reacción adversa, nada grave ni inesperado, pero suficiente para que Pfizer-BioNTech y Moderna tomaran la delantera, con un 95% de eficacia de sus fármacos. Cuando AstraZeneca presentó sus datos también eran muy buenos, pero estaban por detrás y eran confusos: su eficacia media era del 70,4%, con un tipo de dosificación que alcanzaba un 62% y otro que llegaba hasta el 90%. Así que aparecen las dudas y EEUU empieza a descartar esta opción.
Reino Unido –que comenzó a vacunar a principios de diciembre con Pfizer– la aprobó antes de acabar 2020 y la Agencia Europea del Medicamento (EMA) siguió sus pasos. Sin embargo, esta luz verde coincidiría con una tremenda polémica con la Comisión Europea. Bruselas también había apostado fuerte por este proyecto y se veía sin las dosis esperadas. La empresa alega problemas de producción y la Unión Europea publica su contrato: un rifirrafe inaudito entre una farmacéutica y las instituciones comunitarias.
El problema ralentiza los planes de inmunización y no oculta el debate científico: tras el visto bueno de la EMA, uno por uno los países comunitarios van acotando cuál va a ser el uso que le darán a la vacuna y mayoritariamente optan por no vacunar a las personas mayores, precisamente los más vulnerables ante el covid y el principal objetivo en todos los planes de prevención. Para colmo, Sudáfrica suspende por completo la administración del fármaco de AstraZeneca –solo este– al comprobar en datos preliminares correspondientes a los primeros vacunados que la efectividad en población real cae al 22% debido a la variante del coronavirus que circula en el país.
Y a pesar de todos los obstáculos, sigue adelante. Miles de personas están siendo inmunizadas con esta vacuna en Europa –especialmente, en el Reino Unido– y en otros continentes y la Organización Mundial de la Salud (OMS) sale en su defensa, asegurando que es apta para todas las edades. La polémica coincide con la llegada de esta vacuna a España, que prefiere unirse a los países europeos más restrictivos y la reserva para menores de 55 años. La decisión no deja de ser delicada porque nuestro país inicia la vacunación de colectivos que están en primera línea y aún tiene que inmunizar a millones de personas de edades avanzadas. ¿Cuál es la decisión correcta? ¿Aún podemos confiar en este fármaco? Aclaremos todo este caos.
Para leer la nota completa, pulsa aquí
Si quieres recibir en tu celular esta y otras informaciones descarga Telegram, ingresa al link https://t.me/albertorodnews y dale click a +Unirme.