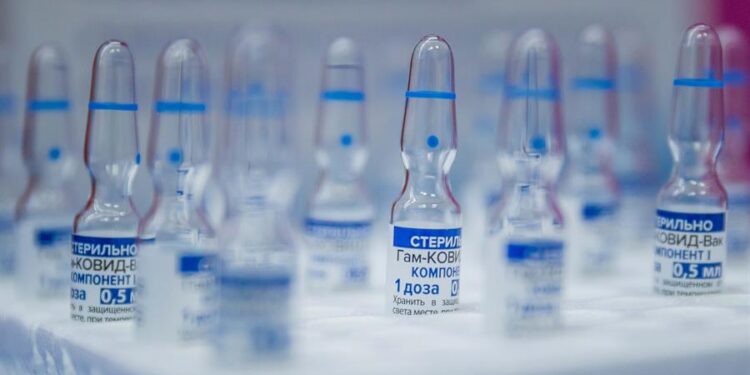
La idea original de este paper encierra una clara paradoja: la misma publicación científica que dio el aval científico y la legitimación de cara a la opinión pública global sobre la evidencia en torno a la seguridad y eficacia de la Fase III de la vacuna Sputnik V contra el COVID-19 – investigada, estudiada y desarrollada por el instituto ruso Gamaleya- ahora queda requebrajada en sus conclusiones y puesta en el banquillo de los acusados en cuanto a la documentación y datos científicos respaldatorios de su fase final, indispensables para que reciba luego la aprobación de las agencias regulatorias globales antes de ser inoculada en seres humanos en una contexto de pandemia global por el virus SARS-COV-2 .
Cabe señalar que aún las dos principales agencias del mundo, la Administración de Medicamentos y Alimentos de los EEUU (FDA) y la Agencia Europea de Medicamentos (EMA) no han aprobado la vacuna de origen ruso.
También es cierto que estas objeciones que en la prestigiosa revista científica The Lancet señalan discrepancias en los datos e informes deficientes en el ensayo de Fase 3 de la vacuna Sputnik V llegan un poco tarde porque la vacuna ya fue aprobada en 64 países, que reúnen una población de más de 3.2 mil millones de personas que la mayoría han sido inoculadas con esta vacuna. Entre estos, la Argentina.
El acceso transparente y disponible a los datos que sustentan los hallazgos de los estudios son imperativos para verificar y confirmar los desarrollos científicos declarados y el acceso restringido dificulta la confianza en las investigaciones. Sin embargo, es aún más grave si hay aparentes errores e inconsistencias numéricas en las estadísticas y los resultados presentados. Lamentablemente, según una investigación publicada en la revista científica The Lancet, esto parece ser lo que está sucediendo en el caso del ensayo de Fase III de la vacuna Sputnik V.
“Hemos realizado varias solicitudes independientes de acceso al conjunto de datos sin procesar, pero nunca fueron respondidas. A pesar de los problemas anteriores y la falta de transparencia, los resultados provisionales del ensayo de Fase III de la vacuna Sputnik V1 nuevamente plantean serias preocupaciones”, reza el estudio publicado en The Lancet.
“Tenemos una gran preocupación -advierten los autores- con respecto a la disponibilidad de los datos, de los cuales los investigadores extraen sus conclusiones. Los investigadores afirman que los datos no se compartirán antes de que se complete el ensayo, y luego solo con la aprobación de las partes interesadas, incluido el llamado departamento de seguridad. El intercambio de datos es una de las piedras angulares de la integridad de la investigación; no debe ser condicional y debe seguir los principios FAIR”.
La segunda preocupación que menciona la investigación se refiere al protocolo del ensayo. “Los investigadores de la Sputnik V mencionan que se agregaron tres análisis provisionales al estudio el 5 de noviembre de 2020, pero este cambio no se registró en ClinicalTrials.gov. Desafortunadamente, el protocolo completo del estudio no se ha puesto a disposición del público, por lo que se desconoce el fundamento de este cambio”.
Según el registro NCT04530396 de ClinicalTrials.gov, el resultado primario se cambió el 17 de septiembre de 2020. Inicialmente, el resultado primario debía evaluarse después de la primera dosis, pero la evaluación se pospuso para después de la segunda dosis. “El resultado primario presentado (eficacia del 91,6%) depende de este cambio, pero las razones del cambio no se han hecho públicas”, sostienen.
“Además de estas enmiendas al protocolo, la definición del resultado primario no está clara en el artículo, donde dice que cuando se sospechó COVID-19, los participantes fueron evaluados con ‘protocolos de diagnóstico de COVID-19, incluida la prueba de PCR’. Aquí, carecemos de información crucial, como los parámetros clínicos que determinan la sospecha de COVID-19, qué protocolos de diagnóstico se usaron, cuándo se realizó la prueba de PCR, qué método específico se usó o cuántos ciclos de amplificación se usaron”, agregan. La forma en que se definieron los casos de sospecha de COVID-19 podría haber provocado un sesgo en las pruebas de PCR utilizadas para evaluar el número de casos confirmados de COVID-19, que es crucial para la determinación de la eficacia.
Otro punto de preocupación sobre el protocolo del estudio se relaciona con el reclutamiento y la asignación al azar de los pacientes. Según el perfil del ensayo, se seleccionaron 35.963 individuos y se asignaron al azar 21.977 individuos. El registro del 20 de enero de 2021 menciona que se inscribieron 33.758 pacientes. Es de esperar que esta última cifra sea igual al número de participantes seleccionados o asignados al azar. Además, no hay información sobre qué causó la exclusión de 13.986 participantes, según el perfil del ensayo.
La tercera preocupación se relaciona con los datos reportados y los resultados numéricos. Los autores del estudio – son nueve calificados cientificos: Enrico M Bucci, Johannes Berkhof , André Gillibert, Gowri Gopalakrishna, Raffaele A Calogero, Lex M Bouter, Konstantin Andreev, Florian Naudet y Vasiliy Vlassov- aseguran haber encontrado las siguientes inconsistencias en los datos: los datos para el grupo vacunado el día 20 se refieren a más personas que el día 10, como si faltara información para 100 participantes el día 10, o si los participantes se inscribieran después del día 10; y el número de participantes informado para las diferentes cohortes de edad vacunadas no se suma al total informado. “Con tales inconsistencias, cuestionamos la exactitud de los datos reportados”, aseveran.
Y concluyen: “Solicitamos una vez más el acceso a los datos de los que se originan las estadísticas para un examen más detenido. Invitamos a los investigadores una vez más a poner a disposición del público los datos en los que se basan sus análisis. El acceso al protocolo, sus enmiendas y los registros individuales de los pacientes es primordial, tanto para la aclaración como para la discusión abierta de todos los temas”.
Fue en febrero de este año cuando The Lancet publicó datos sobre la vacuna rusa Sputnik V: mostró una efectividad de 91,6 % y no registró efectos adversos graves. La prestigiosa revista científica difundió finalmente información técnica de la Fase III del desarrollo del Instituto Gamaleya contra el COVID-19, cuyas dosis son aplicadas en la Argentina y en otros países de América Latina.
A la negativa de FDA y EMA a otorgar la aprobación a la vacuna Sputnik V se sumó bajo el mismo standard la Agencia Nacional de Vigilancia Sanitaria (Anvisa). Hace pocas semanas la reguladora brasileña levantó polvadera cuando justificó por qué no aprobaba la importación de la vacuna rusa al país brasileño: por atribuirle complicaciones en la tecnología utilizada para su producción y en el control de la calidad de las dosis.
El cuestionamiento más grave que la reguladora Anvisa le hace a la vacuna Sputnik V es que a partir de muestras que analizaron, la segunda inyección (el componente adenovirus 5) era “capaz de replicarse”. Lo que significa que una vez dentro del cuerpo, el adenovirus puede continuar multiplicándose.
Consultado hace unas semanas por Infobae, Oscar Cingolani, cardiólogo e investigador de la Universidad Johns Hopkins, no esquivó opinar y reflexionar en el conflicto científico por la seguridad de la vacuna Sputnik V entre Brasil y Rusia. “Involucrarse en estos temas de debate que plantea la ciencia en tiempos de pandemia es una manera de colaborar para lograr información científica transparente, y para el mayor número de personas”, dijo Cingolani desde Maryland.
“Brasil y Rusia deben resolver urgente las objeciones a la seguridad de la vacuna Sputnik V porque atenta contra la certidumbre que necesita la gestión de la pandemia. Y lo deben hacer juntos, en una especie de mesa científica virtual, para exponer las objeciones a la replicación del virus que hace la agencia Anvisa. Y por su lado, el Instituto Gamaleya pueda abrir toda su documentación científica para que, tanto la gente que espera recibir en los próximos días esta vacuna de origen ruso; y entre los que ya están vacunados con Sputnik V puedan quedarse tranquilos y no sentir que su salud está amenazada. Los millones de personas vacunadas en el mundo con la vacuna Sputnik V necesitan tener la tranquilidad de que la inoculación que han recibido es eficaz y segura”, señaló el investigador de Hopkins a Infobae.
Con información de Infobae
Si quieres recibir en tu celular esta y otras informaciones descarga Telegram, ingresa al link https://t.me/albertorodnews y dale click a +Unirme.